I. Notion de synthèse d'une espèce chimique
1. Définition
La synthèse d'une espèce chimique est une transformation chimique au cours de laquelle les réactifs mis en jeu aboutissent à un ou plusieurs produit(s), dont l'espèce chimique recherchée.
Remarque : il est conseillé de réviser la fiche suivante :
2. Propriétés
Le succès d'une synthèse dépend du respect de certaines conditions expérimentales, notamment la pression, la température, la proportion des réactifs, etc.
Si l'espèce chimique synthétisée est identique à une espèce chimique présente dans la nature, alors celle-ci possède les mêmes propriétés physico-chimiques que l'espèce naturelle.
II. Protocole expérimental d'une synthèse
La synthèse d'une espèce chimique s'effectue en plusieurs étapes.
Certaines synthèses sont lentes à température ambiante. L'utilisation d'un chauffage à reflux permet d'accélérer la transformation chimique à température élevée :
Le mélange réactionnel est maintenu à ébullition ;
Les espèces chimiques qui se vaporisent lors du chauffage se condensent (plus exactement se liquéfient) grâce au réfrigérant vertical et refluent donc à l'état liquide vers le ballon ; ceci empêche la perte de réactifs ou de produit(s) due à la vaporisation.
L'agitation est nécessaire pour mélanger les réactifs et pour que le chauffage soit homogène.
Pour séparer l'espèce synthétisée des autres produits éventuellement formés, plusieurs techniques sont possibles (vues au collège) :
Une extraction, si l'espèce chimique synthétisée est mélangée en phase liquide (plusieurs méthodes sont possibles) ;
Une filtration, si l'espèce chimique synthétisée est solide.
Une fois isolée, l'identification de l'espèce chimique synthétisée doit être confirmée par le biais de ses caractéristiques physiques, en particulier :
Sa température de changement d'état ;
Sa masse volumique ;
Son indice de réfraction, par réalisation d'un test chimique ou par chromatographie.
Cette confirmation a pour but de vérifier la pureté de l'espèce chimique synthétisée, de manière à vérifier que la transformation chimique s'est déroulée dans de bonnes conditions.
Pour plus de détails, il est recommandé de relire les fiches suivantes :
III. Application : synthèse d'un arôme de lavande
1. Mise en situation
L'acétate de linalyle est un liquide incolore à l'odeur de lavande.
C'est un arôme qui entre dans la composition de l'huile essentielle de lavande.
Il peut être synthétisé par action du linalol sur l'anhydride acétique.
2. Montage expérimental
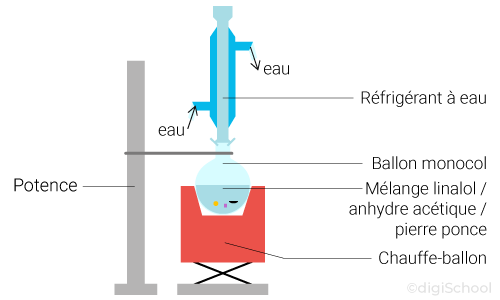
Le schéma ci-dessous est appelé un chauffage à reflux car on chauffe et on refroidit en même temps :
Le linalol et l'anhydride acétique sont les réactifs de cette synthèse.
Pendant la synthèse, le réfrigérant est ouvert car si on le fermait cela pourrait créer une surpression car on chauffe et on refroidit en même temps.
Au cours de cette synthèse, nous allons obtenir de l'acétate de linalyle et de l'acide acétique : ce sont les produits de la réaction.
3. Extraire l'acétate de linalyle
On verse les produits de la réaction dans une ampoule à décanter.
On ajoute par petite quantité 25 mL d'eau. Cet ajout d'eau permet d'éliminer l'anhydride acétique restant et qui se transforme en acide acétique.
La phase organique est constituée d'acétate de linalyle et d'acide acétique, il faut donc éliminer cet acétate de linalyle.
On agite le mélange et on élimine la phase aqueuse qui est plus dense que la phase organique et qui va se retrouver en dessous.
Il reste donc la phase organique avec de l'acide acétique.
Pour l'éliminer, on utilise de l'hydrogénocarbonate de sodium. On verse donc 20 mL d'hydrogénocarbonate de sodium (qui en réagissant avec l'acide acétique, conduit à la formation d'ions acétate et de dioxyde de carbone), puis on attend que le dégagement gazeux ralentisse (ne pas mettre de bouchon sur l'ampoule à décanter sinon il va sauter).
On élimine la phase aqueuse.
Il peut y avoir encore quelque trace d'eau, qui seront éliminées en ajoutant du sulfate de magnésium anhydre.
Enfin, nous avons extrait l'acétate de linalyle.
On peut garder l'acétate de linalyle pour une chromatographie ultérieure.
IV. Conclusion
La chimie de synthèse joue un rôle important dans les domaines de la santé et de l'alimentation et contribue à l'amélioration du confort dans la vie de tous les jours.
= Merci à T_P pour avoir contribué à l'élaboration de cette fiche =