I. Notion d'évolution d'un système chimique
1. Système chimique
Définition :
Un système chimique (ou milieu réactionnel) est un mélange d'espèces chimiques qui sont susceptibles de réagir entre elles.
2. État d'un système chimique
Définitions :
Pour caractériser un système chimique, il est nécessaire de définir l'ensemble des paramètres le constituant, c'est-à-dire :
Les conditions de réalisation de la transformation : la température et la pression ;
Toutes les espèces chimiques mises en jeu : leurs formules brutes et leur(s) état(s) physique(s) (solide (), liquide (), gazeuse () ou dissoute en solution dans l'eau ()) notamment ;
Les quantités de matière de chacune des espèces chimiques mises en jeu (= bilan de matière).
Tous ces paramètres définissent ce qu'on appelle l'état d'un système chimique.
Remarque : les transformations chimiques usuelles se font généralement à l'air libre (sous la pression atmosphérique).
3. La transformation chimique, une évolution d'un système chimique
Définitions :
La transformation (ou réaction) chimique est une évolution d'un système chimique au cours de laquelle des espèces chimiques disparaissent tout en laissant apparaître de nouvelles espèces chimiques ;
Cette caractérisation de l'évolution est permise par la comparaison d'un état initial (i.e. à ) avec un état dit final lorsqu'il n'y a plus de réaction ;
Les espèces chimiques présentes à l'état initial sont appelées réactifs ;
Les espèces chimiques présentes à l'état final sont appelées produits ;
Les espèces chimiques présentes dans le système mais n'étant pas affectées par la transformation sont dites spectatrices.
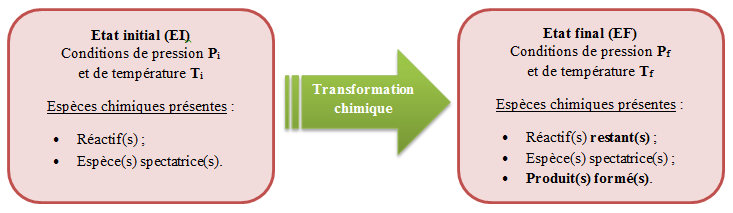
Schématisation d'une transformation chimique :
II. Caractérisation d'une transformation chimique
1. Propriété d'une réaction chimique
Citation :
"Rien ne se perd, rien ne se créé, tout se transforme" (Antoine LAVOISIER, 1743-1794)
Par ces mots, le père de la chimie moderne s'est inspiré du philosophe grec Anaxagore ("Rien ne naît ni ne périt, mais des choses déjà existantes se combinent, puis se séparent de nouveau"). À ceci près que, grâce à ses travaux expérimentaux, celle-ci passe du statut de maxime philosophique à celui de principe physico-chimique.
Propriété :
Une transformation (ou réaction) chimique est caractérisée par une conservation de la matière. Elle se traduit de deux manières :
Conservation de la masse totale du système (autrement dit, conservation du nombre d'atomes des éléments chimiques constituant le système) ;
Conservation de la charge globale du système.
Aspects énergétiques :
Une réaction endothermique est une transformation au cours de laquelle le système chimique (ou milieu réactionnel) absorbe de l'énergie. Généralement, cela se traduit par une diminution de sa température ;
Une réaction exothermique est une transformation au cours de laquelle le système chimique (ou milieu réactionnel) libère de l'énergie. Généralement, cela se traduit par une augmentation de sa température.
2. L'équation d'une réaction chimique : écriture et signification
Définition :
L'équation d'une réaction chimique permet d'établir le bilan des réactifs intervenant dans cette transformation et les produits formés par cette réaction, par le biais de leur formules chimiques ;
Généralement on précise l'état physique de chaque espèce intervenant dans la réaction : solide (), liquide (), gazeux () et aqueux () ;
Elle indique également les proportions des quantités qui interviennent mais pas les conditions de pression et de température dans lesquelles se déroule la réaction.
Exemple :
Remarque importante : les espèces spectatrices, qui n'interviennent pas dans la réaction (c'est-à-dire ne réagissent pas) ne doivent pas apparaître dans l'équation-bilan.
Signification :
Soit l'équation générale d'une réaction chimique .
À l'échelle microscopique : espèce(s) chimique(s) (atome(s), molécule(s) ou ion(s)) réagissent avec espèce(s) chimique(s) pour former espèce(s) chimique(s) et espèce(s) chimique(s) ;
À l'échelle macroscopique : mole(s) de l'espèce chimique réagissent avec mole(s) de l'espèce chimique . Il se forme mole(s) de l'espèce chimique et mole(s) de l'espèce chimique .
Remarque : pour plus d'informations sur la mole, se référer à la fiche suivante :
3. Propriété d'une équation-bilan
L'équation-bilan étant représentative de la transformation étudiée, la propriété de conservation de la matière (en masse et en charge) vue au §II.1 doit donc être respectée.
En conséquence, il est nécessaire d'introduire devant chaque espèce chimique intervenante un nombre qu'on peut ajuster pour traduire cette conservation : on l'appelle le coefficient stœchiométrique.
L'analyse des proportions entre les espèces engagées (= réactifs) et les espèces formées (= produits) est la stœchiométrie.
4. Méthode d'équilibrage d'une équation-bilan
Rappel :
Lors d'une transformation chimique, il y a conservation de la matière (principe de Lavoisier). Cela signifie qu'il doit y avoir autant d'éléments chimiques (C, O, H ...) à gauche (côté réactifs) et à droite (côté produits) de la flèche traduisant l'évolution de la transformation.
Exemple 1 : combustion du charbon () avec le dioxygène () de l'air. Le test à l'eau de chaux permet de dire que le produit est le dioxyde de carbone ().
Dans un premier temps, écrivons cette équation-bilan sans se soucier des équilibres, c'est-à-dire en écrivant uniquement les formules chimiques de chaque réactif et de chaque produit :
Côté réactifs, il y a :
atome de carbone ;
atomes d'oxygène .
Côté produits, il y a :
atome ;
atomes .
L'équation-bilan est donc déjà équilibrée :
Remarque importante : lorsqu'on a qu' seule espèce chimique ou qu' seule mole intervenant dans la réaction, on ne met pas le coefficient stœchiométrique "" devant l'espèce chimique considérée.
Exemple 2 : combustion du propane
En général, l'énoncé donne les formules chimiques de chaque réactif et de chaque produit.
Tout comme l'exemple 1, on écrit l'équation-bilan sans se soucier des coefficients stœchiométriques :
Côté réactifs, il y a :
atomes de carbone (avec le ) ;
atomes d'hydrogène (avec le ) ;
atomes d'oxygène (avec le ).
Côté produits, il y a :
atome de provenant du ;
atomes de provenant du ;
atomes de provenant du et du .
Il n'y a pas autant d'éléments , , de chaque côté de la flèche : l'équation n'est donc pas équilibrée ...
Étape 1 - Équilibrons d'abord les atomes de carbone C :
Pour en avoir pour les réactifs et pour les produits (à la place d'un seul comme on l'a vu précédemment), on multiplie par (car ) :
Étape 2 - Équilibrons ensuite les atomes d'hydrogène :
Pour en avoir pour les réactifs et pour les produits (à la place de comme on l'a vu précédemment), on multiplie par (car ) :
Étape 3 - Il ne reste plus qu'à équilibrer les atomes d'oxygène O. Pour cela, il faut regarder de nouveau l'équation :
Il y en a :
pour les réactifs ;
(pour les ) et (pour les ), c'est-à-dire pour les produits.
Il suffit donc de multiplier par car .
Finalement, l'équation-bilan devient :
5. Pour aller plus loin : bilan d'une réaction chimique
Définition :
L'avancement de la réaction, noté , exprimé en mol, permet de suivre l'évolution des quantités de matières des réactifs et des produits au cours de la transformation chimique ;
Pour une équation chimique du type :
si l'avancement de la réaction est , c'est que les quantités de réactif et de réactif ont été consommées ;
simultanément, les quantités du produit et du produit ont été formées ;
Lors de son arrêt, une transformation chimique est dite totale lorsque qu'un réactif a complètement disparu (ou entièrement réagi) : il est appelé réactif limitant.
Remarque : dans le cas d'une transformation chimique où tous les réactifs ont entièrement réagi, on dit que les réactifs de la réaction chimique considérée ont été introduits dans des proportions stœchiométriques.
Attention : l'état maximal () n'est pas systématiquement atteint ! C'est un état théorique qui permet de déterminer le ou les réactif(s) limitant(s).
= Merci à gbm pour avoir contribué à l'élaboration de cette fiche =