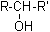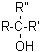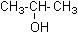I. Molécules de la chimie organique
1. Notion de chimie organique
Définition :
Les molécules de la chimie organique sont principalement constituées des éléments carbone () et hydrogène ().
Ces molécules peuvent également renfermer de l'oxygène (), de l'azote (), voire certains halogènes (tel que le chlore ).
Ce sont des molécules dont les atomes sont liés par des liaisons covalentes.
Historiquement : composé du vivant.
Actuellement : composé de carbone () (sauf , , etc.) avec de l'hydrogène (),
de l'oxygène () et/ou de l'azote ().
Cette forme de chimie sert à analyser et à synthétiser les corps organiques.
2. Groupes caractéristiques et famille chimique
Pour savoir comment trouver la valence des atomes, il est nécessaire de réviser la fiche suivante (§VI) :
Composition d'un système chimique, schéma de Lewis et CLP
Rappel : une liaison covalente est une mise en commun de deux électrons de la couche externe.
Cas de l'atome de carbone :
Son numéro atomique est , ce dernier a donc électrons, répartis de la façon suivante : () ; ce dernier a donc électrons de valence.
Pour satisfaire à la règle de l'octet, l'atome de carbone doit donc compléter sa dernière sous-couche () avec électrons en mettant en commun ses quatre électrons de valence avec d'autres atomes : il est tétravalent et ses quatre liaisons simples s'orientent dans l'espace en faisant entre elles des angles d'environ 109° :
Remarque : un hydrocarbure saturé ne contient que des atomes de carbone tétragonaux. Sinon, il est insaturé.
Une molécule organique, autre que celle d'un hydrocarbure, est constituée :
Du squelette carboné (c'est-à-dire de l'enchaînement des atomes de carbone constituant la molécule), ne comportant que du carbone et de l'hydrogène ;
D'un ou plusieurs groupe(s) caractéristique(s) comptant au moins un atome autre que et (par exemple , , , etc.).
Groupe caractéristique et famille chimique :
Un groupe caractéristique est un groupe d'atomes qui donne des propriétés spécifiques aux molécules qui le possèdent.
On dit que ces molécules (ayant le même groupe caractéristique) forment une famille chimique.
3. Formules chimiques
Formule brute :
La formule brute d'une molécule organique indique les atomes la constituant et leurs quantités respectives.
Exemple : la formule brute du butane s'écrit .
Formule semi-développée plane :
La formule semi-développée d'une molécule organique indique les atomes la constituant sans leurs doublets et les liaisons avec les atomes d'hydrogène () ne sont pas représentées.
Exemple : la formule semi-développée du butane s'écrit .
Formule topologique :
La formule topologique représente la chaîne carbonée par une ligne brisée. Chaque extrémité de segment représente un atome de carbone portant autant d'atomes d'hydrogène qu'il est nécessaire pour satisfaire à la règle de l'octet. Les atomes autres que sont représentés de manière explicite ainsi que les atomes d'hydrogène qu'ils portent (par exemple un groupement ).
Exemple : (le butane) se représente de la manière suivante sous forme topologique :
Remarque : il existe d'autres manières d'écrire les formules chimiques des molécules organiques :
Formule de Lewis ou de Cram : on y voit les atomes ainsi que leurs doublets liants et non-liants. Si nécessaire, aller réviser la fiche suivante :
Représentation de Lewis et géométrie des molécules et des ions
Conformation : arrangement spatial des atomes d'une molécule qui peut être modifié par rotation autour des liaisons simples. Par exemple, le butane peut exister sous différentes conformations (éclipsée, décalée).
Formule développée plane : elle est identique à la formule de Lewis, mais les doublets non-liants ne sont pas visibles. Elle précise la nature et l'ordre d'enchaînement des liaisons entre les différents atomes d'une molécule ;
II. Les chaînes carbonées saturées
1. Définitions
On appelle chaîne carbonée principale la partie linéaire du squelette la plus longue. C'est elle qui va définir le nom de l'hydrocarbure.
Une liaison simple est dite saturée. Une chaîne carbonée qui ne comporte que des liaisons simples "" est saturée et les carbones sont tétragonaux.
Une chaîne est linéaire quand un carbone est lié au plus à deux carbones (si le squelette ne comporte que des atomes alignés).
Une chaîne est dite ramifiée lorsqu'elle est composée au moins d'un carbone lié à trois ou quatre atomes de carbone (on a donc des groupes d'atomes sur la chaîne principale).
Enfin, on parle d'une chaîne cyclique quand elle ne comporte que des carbones liés à au moins deux autre carbone (on observe alors une chaîne fermée en forme de polygone).
2. Les alcanes à chaîne linéaire : nomenclature
Formule brute de l'alcane à chaîne linéaire :
Les alcanes constituent la famille des molécules de formule brute de la forme :
( étant un nombre entier)
Nomenclature : leur nom est constitué d'un radical qui dépend de la longueur de la chaîne suivi du suffixe "-ane". Les quatre premiers termes ont des noms usuels :
Méthane : ;
Éthane : ;
Propane : ;
Butane : .
Les termes suivants ont un nom formé d'un préfixe qui indique le nombre d'atomes de carbone et du suffixe "-ane" :
Pentane : ;
Heptane : .
3. Le groupe substituant : les alkyles
Formule brute de l'alkyle :
L'alkyle est un substituant qui dérive d'un alcane en retirant à ce dernier un hydrogène. Sa formule brute est :
Son nom dérive de celui de l'alcane ayant le même nombre de carbone(s) : on remplace le suffixe "-ane" par "-yle".
Exemple : est le groupement méthyle.
4. Nomenclature des alcanes ramifiés
Alcane ramifié :
Lorsque les alcanes sont constitués d'une chaîne linéaire carbonée sur laquelle sont liés les alkyles : on dit qu'ils sont ramifiés.
On repère la chaîne la plus longue car le radical dépend du nombre d'atomes de cette chaîne. On ajoute ensuite un préfixe qui permet de nommer les ramifications.
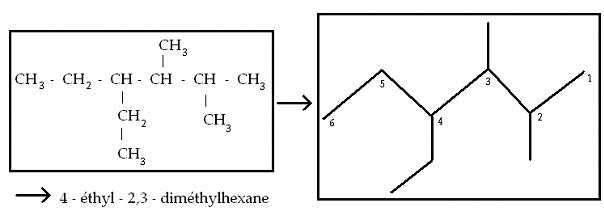
Exemple :
Méthode : on peut donner un nom à l'espèce ci-dessus. Pour ce faire, il faut, dans l'ordre :
Trouver une chaîne avec le plus grand nombre de carbones possible (ici, il y en a : c'est donc un composé de l'hexane).
Reconnaître des groupes alkyles existants. On remarque alors qu'au deuxième carbone en partant de la droite ainsi qu'au troisième, on reconnaît un groupe "Méthyl". De même, il y a un groupe "Ethyl" au quatrième carbone.
On peut alors donner le nom suivant : 4-éthyl-2,3-diméthylhexane (on dit diméthyl car il y a deux groupes "Méthyl").
III. Les chaînes carbonées insaturées
Chaîne carbonée insaturée :
Lorsqu'une molécule comporte au moins une double liaison, on dit qu'elle est insaturée.
Remarque :
Les liaisons multiples sont dites insaturées (liaisons doubles ou triples).
Les chaînes carbonées insaturées contiennent donc au moins une liaison insaturée.
1. Les alcènes
Définition :
Les alcènes sont des hydrocarbures qui renferment une ou plusieurs liaison(s) double(s) (que la chaîne carbonée soit linéaire ou ramifiée) et ayant pour formule brute .
Nomenclature : on considère le nom de l'alcane correspondant (c'est-à-dire le même squelette carboné mais sans double liaison) pour lequel on remplace "ane" par "ène". Il faut repérer l'emplacement de la double liaison et le numéro du premier atome de carbone qui la porte. On intercale le numéro de ce carbone entre le radical et le suffixe "ène".
Exemples :
est le but-1-ène ;
est le but-2-ène ;
2. Les alcynes
Définition :
Les alcynes sont des hydrocarbures possédant une ou plusieurs liaison(s) triple(s).
Nomenclature : idem que pour les alcènes, mais l'on change "-ène" en "-yne".
IV. Les familles de molécules oxygénées
1. Rappels : l'oxygène et ses liaisons
Son numéro atomique est , ce dernier a donc électrons, répartis de la façon suivante : () ; ce dernier a donc électrons de valence.
Pour satisfaire à la règle de l'octet, l'atome de carbone doit donc compléter sa dernière sous-couche () avec électrons en mettant en commun ses deux électrons de valence avec d'autres atomes : il est divalent. Il peut donc établir liaisons covalentes : soit avec deux atomes différents, soit avec le même atome (liaison double).
2. Les alcools
Formule brute des alcools :
Les molécules des cette famille des alcools présentent toutes un groupe hydroxyle fixé sur leur chaîne carbonée.
Les alcools à chaîne carbonée saturée ont pour formule générale :
On dénombre trois types d'alcool :
Les alcools primaires (alcools I) ;
Les alcools secondaires (alcools II) :
Les alcools tertiaires (alcools III) :
Exemples :
L'éthanol : CH-CH-OH (alcool I) ;
Le propan-2-ol (alcool II) :
Le 2-méthylpropan-2-ol (alcool III) :
Différenciation des trois classes d'alcools : par oxydation ménagée (sans destruction du squelette carboné de la molécule oxydée) en présence des ions permanganate ou dichromate en milieu acide. Ainsi :
Un alcool primaire oxydé donne une aldéhyde puis après une nouvelle oxydation un acide carboxylique ;
Un alcool secondaire oxydé donne une cétone ;
Un alcool tertiaire n'est pas oxydé.
Test caractéristique : test au permanganate de potassium. L'alcool est oxydé, l'ion permanganate est réduit en ion manganèse. La solution devient incolore.
Nomenclature : le nom est formé d'un préfixe décrivant la chaîne carbonée suivi de l'indice de position du groupe hydroxyle plus la terminaison "ol".
3. Les composés carbonylés (aldéhydes et cétones)
Les composés carbonylés sont des molécules organiques qui contiennent le groupe carbonyle .
Il existe deux familles :
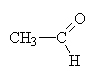
Les aldéhydes : le groupe carbonyle est lié à un atome d'hydrogène. On obtient la fonction en bout de chaîne.
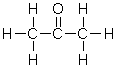
Les cétones : le groupe carbonyle est lié à deux atomes de carbone. Le groupement se trouve donc au sein de la chaîne carbonée, on a .
Exemples :
L'éthanal :
La propanone également appelée acétone :
Tests caractéristiques :
Commun aux composés carbonylés : le réactif utilisé est la 2,4-DNPH (2,4-DiNitroPhénylHydrazine). On observe la formation d'un précipité orange de 2,4-dinitrophénylhydrazone lorsque le test est positif.
Caractérisation des aldéhydes :
Test à la liqueur de Fehling : en chauffant elle passe du bleu au rouge brique si le test est positif.
Test au réactif de Tollens (ou test du miroir d'argent) : une solution ammoniacale d'ions argent est mélangée à l'aldéhyde. Les ions Ag sont réduits en argent métallique qui se dépose sur les parois du récipient.
Test au réactif de Schiff (solution de fuschine décolorée par le dioxyde de soufre) : en présence d'une aldéhyde, elle prend une teinte rose-violacée.
Nomenclature : on remplace la terminaison "e" de l'alcane par
"al" pour un aldéhyde ;
"one" pour une cétone.
4. Les acides carboxyliques
Formule brute des acides carboxyliques :
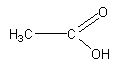
Les acides carboxyliques ont pour formule semi-développée ou, plus simplement, . Le groupe caractéristique carboxyle est en bout de chaîne.
Exemple : l'acide éthanoïque
Tests caractéristiques : mesure du pH (pH-mètre ou stylo-pH), utilisation de papier pH, indicateur coloré.
Nomenclature : leur appellation dans la nomenclature officielle dérive de l'alcane associé . On ajoute le mot "acide" devant le nom de l'hydrocarbure correspondant et on remplace le "e" final par le suffixe "oïque".
5. Les amines
Les amines sont des molécules qui contiennent le groupe caractéristique amino . Il s'agit de composés azotés dérivant de l'ammoniac par remplacement d'un ou plusieurs atomes d'hydrogène par des groupes carbonés.
Les amines à chaîne carbonée saturée ont pour formule générale .
Par analogie avec les alcools, la classe de l'amine est définie par le nombre d'atomes d'hydrogène liés à l'azote : on distingue ainsi les amines primaires (I), secondaires (II) et tertiaires (III).
Exemples :
Le méthanamine est une amine I : ;
Le N-méthylméthanamine est une amine II : ;
Le triméthylamine de formule est une amine III :
Test caractéristique : test de (ce sont des espèces basiques en solution aqueuse). Elles font partie des couples acido-basiques ion alkylammonium / amine ( / ). Elles réagissent avec l'eau selon l'équation :
Ce sont les ions hydroxyde les responsables de la basicité en solution aqueuse.
Nomenclature : leur nom officiel s'obtient en remplaçant le "e" final de l'alcane dont il dérive par le suffixe amine. Une nomenclature plus courante (nomenclature radico-fonctionnelle) consiste à ajouter le suffixe amine au nom du radical après en avoir supprimé le "e" final.
Remarque : la fonction amine recouvre un ensemble très étendu de composés, par exemple :
Les acides aminés comme l'acide 2-aminopropanoïque également appelé alanine ;
Les alcaloïdes comme la caféine :
6. Cas particulier des acides α-aminés et acides gras
Acides α-aminés : ce sont des molécules contenant à la fois un groupe amine () et un groupe acide carboxylique (). Ils sont les constituants des protéines.
Acides gras : ce sont des acides carboxyliques à longue chaîne carbonée (souvent à atomes de carbone). Ils sont importants dans la structure des graisses et des huiles.
V. Isomérie de constitution
1. Notion d'isomérie
Des molécules sont dites isomères si elles sont différentes mais ont des formules brutes identiques.
Remarque : les molécules de deux isomères ne sont pas superposables.
2. Les isomères de constitution
Des isomères de constitution ont la même formule brute mais des formules planes différentes (les squelettes carbonés sont différents).
On distingue plusieurs types d'isomères de constitution :
Les isomères de chaîne : seul le squelette carboné change. Par exemple : .
Les isomères de position où un groupe caractéristique ou une instauration occupe une position différente sur un squelette carboné inchangé. Par exemple : .
Les isomères de fonction pour lesquels le groupe caractéristique diffère. Par exemple, l'éthanol et l'étheroxyde .
VI. Atome de carbone asymétrique et énantiomérie
Définitions :
Un atome de carbone asymétrique est un atome de carbone lié à quatre groupes d'atomes différents. Il est noté .
Énantiomérie : deux molécules sont dites énantiomères si elles sont images l'une de l'autre dans un miroir et ne sont pas superposables.
Exemple : Le 2-butanol a un carbone asymétrique et existe sous deux formes énantiomères.
= Merci à shadowmiko / JBT / gbm pour avoir contribué à l'élaboration de cette fiche =