I. Oxydant, Réducteur et nombre d'oxydation
1. Notions d'oxydant et de réducteur
Définitions :
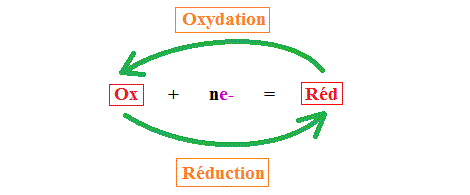
Un oxydant est une espèce chimique capable de capter un ou plusieurs électron(s), notés .
Un réducteur est une espèce chimique capable de céder un ou plusieurs électron(s), notés .
2. Nombre d'oxydation
Définition :
Le nombre d'oxydation (ou degré d'oxydation) d'un élément dans une espèce chimique est un nombre qui permet de suivre le transfert d'électrons au cours d'une réaction. Il est défini comme la charge électrique que porterait l'élément si toutes les liaisons étaient ioniques.
Règles pour déterminer le nombre d'oxydation :
Dans une molécule neutre, la somme des nombres d'oxydation de tous les atomes est nulle ;
Dans un ion polyatomique, la somme des nombres d'oxydation de tous les atomes est égale à la charge de l'ion.
Exemples :
L'oxygène a généralement un nombre d'oxydation de (sauf dans les peroxydes où il est ) ;
Dans l'ion sulfate (), l'oxygène a un nombre d'oxydation de . La somme des nombres d'oxydation est (charge de l'ion).
Donc, pour le soufre :
Le nombre d'oxydation du soufre est donc ;
L'hydrogène a généralement un nombre d'oxydation de (sauf dans les hydrures métalliques où il est ) ;
Les métaux alcalins (groupe 1) ont un nombre d'oxydation de ;
Les métaux alcalino-terreux (groupe 2) ont un nombre d'oxydation de .
II. Les couples oxydant/réducteur
Définition :
Deux espèces chimiques forment un couple oxydant/réducteur si on peut passer de l'un à l'autre par une perte ou un gain d'un ou plusieurs électrons .
Un couple oxydant-réducteur s'écrit de la manière suivante : .
Ces deux espèces chimiques sont dites conjuguées : est l'oxydant conjugué de et est le réducteur conjugué de .
Exemples :
: est l'oxydant et est le réducteur de ce couple ;
;
;
.
III. Demi-équation d'oxydo-réduction
Soit un couple oxydant/réducteur , on passe de l'un à l'autre par perte ou gain d'un ou plusieurs électron(s) :
Si l'oxydant est le réactif alors l'équation s'écrira : , où est le nombre d'électron(s) capté(s) ;
Si le réducteur est le réactif alors l'équation s'écrira : , où est le nombre d'électron(s) cédé(s).
IV. Réaction d'oxydoréduction
1. Définition et propriété d'une réaction d'oxydoréduction
Définition :
La réaction d'oxydoréduction est caractérisée par un transfert d'électrons par contact entre un oxydant et un réducteur de deux couples différents.
Lors d'une réaction d'oxydoréduction, il y a deux couples oxydant/réducteur qui interviennent : et .
L'oxydant d'un couple réagit avec le réducteur du deuxième couple.
On fait réagir l'oxydant avec le réducteur .
En écrivant les 2 demi-équations d'oxydoréduction, on obtient :
( est le nombre d'électron(s) capté(s)) ;
( est le nombre d'électron(s) cédé(s)).
Propriété :
Dans une réaction d'oxydoréduction, il faut que le nombre d'électron(s) cédé(s) et le nombre d'électron(s) capté(s) soit le même.
Méthode :
Si le nombre d'électrons est le même, il n'y a aucun changement à faire.
Si le nombre d'électrons dans chaque demi-équation est différent, il faut multiplier les demi-équations par un entier pour obtenir le même nombre d'électrons.
Pour ce faire, on multiplie la première équation par un entier et on multiplie la deuxième équation par un autre entier de telle sorte que le nombre d'électrons transférés soit le même dans les deux demi-équations.
L'équation de la réaction sera : .
Remarque importante : on ne fait pas figurer les électrons dans l'équation, puisqu'on a équilibré chaque demi-équation en nombre égal d'électron(s).
2. Application simple : réaction de l'aluminium dans une solution de sulfate de cuivre
On introduit des morceaux d'aluminium dans une solution de sulfate de cuivre. L'aluminium va donc réagir avec l'ion .
Les couples en présence sont et .
Les demi-équations des deux couples qui réagissent sont :
;
.
On remarque que le nombre d'électrons n'est pas le même, on va donc multiplier la première demi-équation par et la deuxième demi-équation par , on aura donc électrons :
;
.
Finalement, l'équation de la réaction sera :
3. Cas où la réaction d'oxydoréduction ne se fait pas que par un simple transfert d'électrons
Il y a des cas où trouver la demi-équation s'avère un peu plus délicat.
En effet, avec certaines espèces chimiques, telles que l'ion permanganate et le manganèse, on ne peut pas passer de l'un à l'autre par un simple transfert d'électrons.
Des molécules d'eau et des protons () apparaissent dans la demi-équation.
Prenons l'exemple de l'ion permanganate et du manganèse dont le couple est .
Étape 1 : on commence à écrire ceci :
On vérifie si l'élément chimique est équilibré (ici oui, un de chaque côté)
Étape 2 : on a oxygène à gauche, il en faut aussi à droite.
Pour cela, on rajoutera donc molécules d'eau, chaque molécule apportant un oxygène :
Étape 3 : il y a 8 atomes d'hydrogène à droite (par l'ajout des molécules d'eau), on équilibre donc à gauche en rajoutant des protons (ou ions oxonium ) :
Étape 4 : pour finir, on équilibre le nombre de charges, 7+ à gauche et 2+ à droite, en rajoutant donc 5 électrons à gauche :
V. Oxydant réduit et réducteur oxydé
Définitions :
Durant la réaction d'oxydo-réduction :
L'oxydant est réduit, il gagne des électrons : (= réduction)
Le réducteur est oxydé, il perd des électrons : (= oxydation).
VI. Les piles électrochimiques
1. Transfert spontané d'électrons
Expérience :
Chaque bécher contient les deux espèces d'un couple oxydant/réducteur ;
Le schéma de principe de la pile Daniell est le suivant :
Définitions :
Une demi-pile est l'ensemble constitué par les deux espèces d'un couple .
Une pile comporte toujours deux demi-piles dont les électrolytes sont reliées par un conducteur ionique (pont électrolytique ou vase poreux).
Pour qu'une pile fonctionne, il faut que les lames métalliques, appelées électrodes, soient reliées par une suite continue de conducteurs métalliques.
On constate qu'un courant d'intensité traverse la résistance en allant de la lame vers la lame .
Interprétation :
Les lames métalliques, les fils de jonction, l'ampèremètre, la résistance sont parcourus par des électrons libres qui se déplacent en sens inverse du courant.
Les solutions ioniques sont le siège d'un double déplacement d'ions :
Les anions se déplacent vers l'anode, en sens inverse du courant ;
Les cations se déplacent vers la cathode, dans le sens du courant.
Au niveau de la lame de , des électrons sont donnés au circuit par oxydation des atomes de :
Au niveau de la lame de , des électrons venant du circuit sont consommés par réduction des ions :
Ainsi, l'échange d'électrons entre et se fait de façon indirecte, par l'intermédiaire du circuit extérieur. C'est à la surface des électrodes que se font les échanges d'électrons.
Le bilan de cet échange est :
L'évolution du système se fait dans le sens direct sans contact entre les réactifs, mais la boucle conductrice doit être fermée.
2. Constitution et fonctionnement d'une pile
Une pile est constituée de deux demi-piles reliées par un pont ionique qui assure la neutralité électrique de chaque solution.
Pour fonctionner, la pile doit être placée dans un circuit électrique fermé par un conducteur métallique qui permet un transfert d'électrons entre un oxydant d'un couple et le réducteur d'un autre couple.
Définition :
La force électromotrice (ou fém) d'une pile est la tension entre le pôle positif et le pôle négatif de cette pile à vide (quand elle ne débite pas de courant).
Exemple de la pile Daniell :
Pour cette pile, la fém est ;
Quand la pile fonctionne, le courant circule dans le circuit du pôle positif, électrode de cuivre, vers le pôle négatif, électrode de zinc ;
Les électrons circulent dans le sens inverse : du pôle négatif au pôle positif.
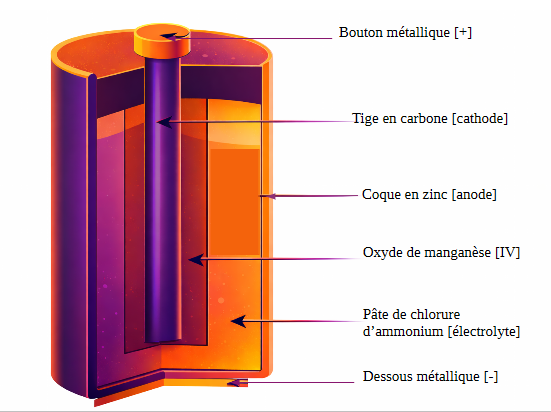
3. Les piles usuelles
On peut évoquer par exemple :
La pile saline ;
La pile alcaline ;
La pile à combustible ;
Etc.
4. Différence entre les piles et les accumulateurs
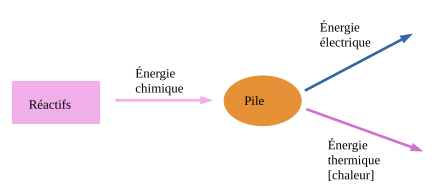
Pour rappel, une pile est un dispositif électrochimique qui convertit l'énergie chimique en énergie électrique. Elle fonctionne grâce à une réaction d'oxydoréduction spontanée et ne peut pas être rechargée.
Un accumulateur est un système électrochimique qui peut être rechargé en lui fournissant de l'énergie électrique, permettant de stocker de l'énergie chimique pour une utilisation ultérieure.
Différences fondamentales entre une pile et un accumulateur :
Une pile est à usage unique (non rechargeable) ;
Un accumulateur est rechargeable et peut subir plusieurs cycles de charge et décharge.
Exemples :
Une pile AA alcaline est jetable après utilisation ;
Une batterie de smartphone (accumulateur lithium-ion) peut être rechargée des centaines de fois.
VII. Quantité d'électricité débitée par une pile et quantités de matière mises en jeu
Remarque : cette partie de la fiche de cours a un lien avec celle-ci (§VI) :
1. Quantité d'électricité débitée par une pile
La quantité d'électricité mise en jeu au cours du fonctionnement d'une pile est égale à la charge totale des électrons échangés :
avec
quantité d'électrons échangés au cours du fonctionnement d'une pile ;
la constante d'Avogadro ;
la charge élémentaire.
Le faraday est la valeur absolue de la charge d'une mole d'électrons ou quantité d'électricité transportée par une mole d'électrons :
Ainsi, .
La quantité d'électricité que fait circuler une pile qui débite un courant d'intensité pendant une durée est :
La capacité d'une pile est la quantité d'électricité maximale que cette pile peut fournir.
2. Quantités de matière mises en jeu : application
Enoncé :
Au cours du fonctionnement d'une pile Daniell, la masse de l'électrode du zinc diminue de en .
Quelle est l'intensité du courant constant débitée ?
Solution :
Le symbole conventionnel de la pile Daniell est ;
La masse de zinc consommée est ;
La durée de fonctionnement de la pile est ;
L'équation de la réaction qui se produit à l'électrode de zinc est ;
La quantité de matière de zinc qui a été consommée est :
La quantité de matière d'électrons qui a circulé est ;
La quantité d'électricité qui a circulé est ;
La pile a fait circuler cette quantité d'électricité pendant la durée donc l'intensité du courant débitée par la pile est :
Application numérique :
;
;
;
.
donc
3. Conversion d'énergie chimique en énergie électrique
Dans une pile ou un accumulateur, la conversion d'énergie chimique en énergie électrique repose sur des réactions d'oxydoréduction qui se produisent aux électrodes.
Au niveau de l'anode, une oxydation se produit (= perte d'électrons).
Au niveau de la cathode, une réduction se produit (= gain d'électrons).
Les électrons circulent à travers un circuit externe, produisant un courant électrique.
La réaction globale peut s'écrire :
L'énergie chimique stockée est convertie en énergie électrique selon la relation :
où :
est l'énergie en joules (),
est la quantité d'électricité en coulombs (),
est la tension entre les bornes en volts ().
= Merci à gbm / Skops pour avoir contribué à l'élaboration de cette fiche =