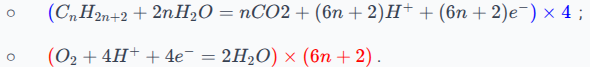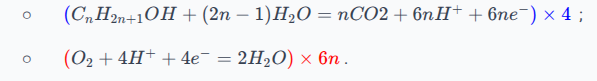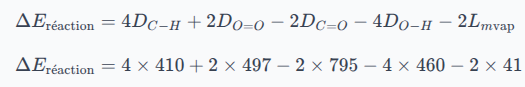I. Rappels de première
La présente fiche s'inscrit dans la continuité des notions vues en classe de première :
Système chimique (ou milieu réactionnel) ;
État d'un système chimique ;
Transformation (ou réaction) chimique, avec les réactifs, les produits et les espèces spectatrices ;
Le principe de conservation d'une transformation chimique en masse et en charge totale ;
Réactions endothermique et exothermique.
Il est donc essentiel de relire la fiche de cours suivante pour réviser ces notions :
Les autres notions introduites en première seront revues dans la présente fiche.
II. Combustion des matières organiques : rappels
1. Notion de combustion
Définition :
Une combustion est une transformation chimique d'oxydoréduction au cours de laquelle le système libère de l'énergie : c'est une réaction exothermique. Elle s'accompagne donc d'une hausse systématique de température du milieu extérieur.
2. Réactifs et produits d'une combustion
Une combustion se caractérise par le contact de deux réactifs :
Le combustible, qui est l'espèce chimique qui brûle ; c'est celui des réactifs qui a subi une oxydation.
Le comburant, qui est l'espèce chimique qui aide le combustible à brûler (généralement il s'agira du dioxygène ). C'est celui des réactifs qui a subi une réduction.
Propriété :
Lors d'une combustion complète, tout le combustible a réagi (= réaction totale, le dioxygène étant généralement en excès) et les produits formés sont le dioxyde de carbone () et l'eau ().
3. Combustibles organiques usuels
Les combustibles utilisés dans la vie quotidienne sont essentiellement d'origine fossile. Ils résultent de la décomposition d'organismes vivants effectuée pendant plusieurs millions d'années.
Les alcanes et les alcools sont privilégiés comme combustibles car ils ont une forte énergie massique ou volumique :
Le gaz naturel est composé d'hydrocarbures gazeux constitués de méthane (en grande majorité), d'éthane , de propane et de butane . Il est rendu odorant par l'ajout de THT (tétrahydrothiophène) ;
Certaines cheminées ou poêles fonctionnent à l'éthanol .
III. Réaction de combustion des alcanes et des alcools : rappels
1. Réaction de combustion d'un alcane ou d'un alcool
Comme nous l'avons vu précédemment, la réaction de combustion d'un alcane ou d'un alcool est une réaction d'oxydoréduction entre l'une des deux espèces organiques et le dioxygène, les produits formés étant le dioxyde de carbone et l'eau.
Remarque : pour plus d'information sur une réaction d'oxydoréduction, se référer à la fiche suivante :
Ces réactions exothermiques s'effectuant à des températures élevées, on suppose que cette transformation entre ses réactifs et ses produits se fait à l'état gazeux.
2. Équation-bilan d'une réaction de combustion
Les couples en jeu sont :
;
.
Les demi-équations électroniques, dans le sens de la réaction effective, sont les suivantes :
;
.
On remarque que le nombre d'électrons n'est pas le même, on va donc multiplier la première demi-équation par et la deuxième demi-équation par , on aura donc électrons :
Finalement, l'équation de la réaction (une fois simplifiée) sera :
Les couples en jeu sont :
;
.
Les demi-équations électroniques, dans le sens de la réaction effective, sont les suivantes :
;
.
On remarque que le nombre d'électrons n'est pas le même, on va donc multiplier la première demi-équation par et la deuxième demi-équation par , on aura donc électrons :
Finalement, l'équation de la réaction (une fois simplifiée) sera :
Généralement, il ne sera pas nécessaire de refaire toutes les étapes d'écriture d'une équation-bilan d'oxydoréduction.
L'équation générale d'une combustion complète d'un hydrocarbure (combustible contenant uniquement du carbone et de l'hydrogène) peut-être simplifiée de la façon suivante :
En effet, on peut équilibrer ces réactions directement en commençant par équilibrer le carbone et l'oxygène et en terminant par l'hydrogène, selon le principe de Lavoisier. Pour cela, il est conseillé de lire attentivement le §II. 4. de la fiche suivante :
Combustion du propane : (l'équilibrage de cette équation-bilan est détaillé dans la fiche ci-dessus) ;
Combustion de l'éthanol : .
VI. Énergie libérée au cours d'une combustion
1. Énergies disponibles dans une molécule
La formation d'une liaison covalente entre deux atomes est une transformation qui conduit à libérer de l'énergie : on dit qu'il s'agit d'un processus exothermique. A l'inverse, la rupture d'une liaison covalente entre deux atomes d'une molécule requiert de l'énergie (dite énergie de liaison) : on dit qu'il s'agit d'un processus endothermique.
Définition :
Pour une liaison covalente entre deux atomes, l'énergie de liaison est égale à l'énergie nécessaire pour rompre une mole de cette liaison entre les deux atomes pris à l'état gazeux : ;
Elle s'exprime en kilojoules par mole ( ou ) ;
Plus la liaison à rompre est forte, plus la quantité d'énergie qu'il faudra fournir est importante. Cette énergie à fournir peut par exemple l'être sous forme thermique.
Propriété :
Au cours d'une transformation chimique, des liaisons covalentes sont rompues et d'autres sont formées.
Définition :
L'énergie molaire de cohésion est égale à l'énergie nécessaire à une mole d'une molécule pour la dissocier en tous ses atomes constitutifs. En d'autres termes, elle est égale à la somme de toutes les énergies de liaison entre les atomes constituant cette molécule.
Ainsi, si on note l'énergie de la liaison covalente entre deux atomes et , on peut écrire :
Elle s'exprime donc également en kilojoules par mole ( ou ).
2. Énergie molaire de la réaction de combustion
Définition :
Au cours d'une combustion, l'énergie molaire de la réaction correspond au bilan des énergies consommées (= liaisons dans le combustible et le comburant - les réactifs - qui se rompent) et libérées (= énergies dans le dioxyde de carbone et l'eau - les produits - qui se forment) ;
Elle correspond donc à la somme algébrique des énergies de liaisons rompues et formées sur la base de l'équation-bilan de la combustion :
Exemple de la combustion du méthane :
L'équation-bilan de la réaction de combustion est :
Si on décompose cette combustion :
Les liaisons du méthane sont rompues ;
La liaison du dioxygène est rompue ;
Les liaisons du dioxyde de carbone sont formées ;
Les liaisons de l'eau sont formées ;
Étant donnée que les énergies de liaisons sont prises à l'état gazeux, il faut tenir compte d'un changement d'état pour l'eau : il s'agit d'une chaleur latente (ou énergie massique de changement d'état) de liquéfaction (= l'inverse de la chaleur latente de vaporisation). En cas de besoin, se référer à la fiche suivante :
En tenant compte des coefficients stœchiométriques, l'énergie molaire de la réaction de combustion du méthane s'écrit :
3. Cas de la combustion des alcanes et des alcools en phase gazeuse
Avec l'exemple traité ci-dessus, on constate que l'énergie molaire d'une réaction de combustion est négative. Cela permet donc de confirmer que de l'énergie est libérée au cours de cette transformation : c'est bel et bien une réaction exothermique.
La totalité de cette énergie cédée à l'extérieur du système chimique l'est sous forme thermique.
Définition :
Connaissant la quantité de matière de combustible introduite dans une réaction de combustion complète (= en supposant que celle-ci sera totale), l'énergie libérée au cours de cette combustion s'écrit :
est l'énergie libérée lors de la combustion (en ) ;
est la quantité de matière du combustible introduite dans la combustion (en ) ;
est l'énergie molaire de la réaction de combustion étudiée (en ).
Définition :
Le pouvoir calorifique d'un alcane ou d'un alcool, noté correspond à l'énergie thermique libérée par une combustion complète de 1 kg de combustible ;
C'est l'opposé de l'énergie libérée au cours d'une réaction de combustion par unité de masse.
C'est donc une grandeur positive, qui s'exprime généralement en ou .
Remarque : cette notion avait été introduite en classe de première :
V. Combustions et enjeux de société
Les combustions et enjeux de société ont été abordés en classe de première dans la fiche de cours suivante :
VI. Applications concrètes
Étude comparée de la combustion d'une chaudière avec ou sans condensation :
Analyser les différences d'efficacité énergétique entre une chaudière à condensation (récupérant la chaleur latente de la vapeur d'eau) et une chaudière classique ;
Calculer le gain énergétique et l'impact sur les émissions de .
Étude comparée de dispositifs de chauffage à combustion :
Comparer l'efficacité énergétique, le bilan carbone, et le coût de différents dispositifs (chaudière au gaz, pompe à chaleur, chauffage électrique) ;
Évaluer les émissions de par produit pour chaque dispositif.
Impact environnemental des combustions :
Calculer la quantité de produite par la combustion d'une masse donnée de combustible ;
Exemple : la combustion de de méthane produit de .
Exploitation des courbes et données expérimentales :
Les courbes de combustion fournissent des données expérimentales sur l'énergie libérée en fonction du temps ou de la quantité de combustible brûlé ;
Exploiter ces courbes pour déterminer :
La puissance thermique instantanée ;
L'énergie totale libérée ;
Le rendement énergétique du dispositif de combustion.
= Merci à athrun pour avoir contribué à l'élaboration de cette fiche =