I. Rappels de première
La présente fiche s'inscrit dans la continuité des notions vues en classe de première :
Oxydant et réducteur ;
Couple oxydant / réducteur ;
Demi-équation et réaction d'oxydoréduction ;
Méthodes d'équilibrage des réaction d'oxydoréduction ;
Les piles électrochimiques (dont les usuelles).
Il est donc essentiel de relire la fiche de cours suivante pour réviser ces notions :
Réaction d'oxydoréduction, corrosion et piles
1. Transfert spontané d'électrons
Expérience :
Chaque bécher contient les deux espèces d'un couple oxydant/réducteur ;
Le schéma de principe de la pile Daniell est le suivant :
Définitions :
Une demi-pile est l'ensemble constitué par les deux espèces d'un couple .
Une pile comporte toujours deux demi-piles dont les électrolytes sont reliées par un conducteur ionique (pont électrolytique ou vase poreux).
Pour qu'une pile fonctionne, il faut que les lames métalliques, appelées électrodes, soient reliées par une suite continue de conducteurs métalliques.
On constate qu'un courant d'intensité traverse la résistance en allant de la lame vers la lame .
Interprétation :
Les lames métalliques, les fils de jonction, l'ampèremètre, la résistance sont parcourus par des électrons libres qui se déplacent en sens inverse du courant.
Les solutions ioniques sont le siège d'un double déplacement d'ions :
Les anions se déplacent vers l'anode, en sens inverse du courant ;
Les cations se déplacent vers la cathode, dans le sens du courant.
Au niveau de la lame de , des électrons sont donnés au circuit par oxydation des atomes de :
Au niveau de la lame de , des électrons venant du circuit sont consommés par réduction des ions :
Ainsi, l'échange d'électrons entre et se fait de façon indirecte, par l'intermédiaire du circuit extérieur. C'est à la surface des électrodes que se font les échanges d'électrons.
Le bilan de cet échange est :
L'évolution du système se fait dans le sens direct sans contact entre les réactifs, mais la boucle conductrice doit être fermée.
2. Constitution et fonctionnement d'une pile
Une pile est constituée de deux demi-piles reliées par un pont ionique qui assure la neutralité électrique de chaque solution.
Pour fonctionner, la pile doit être placée dans un circuit électrique fermé par un conducteur métallique qui permet un transfert d'électrons entre un oxydant d'un couple et le réducteur d'un autre couple.
Définition :
La force électromotrice (ou fém) d'une pile est la tension entre le pôle positif et le pôle négatif de cette pile à vide (quand elle ne débite pas de courant).
Exemple de la pile Daniell :
Pour cette pile, la fém est ;
Quand la pile fonctionne, le courant circule dans le circuit du pôle positif, électrode de cuivre, vers le pôle négatif, électrode de zinc ;
Les électrons circulent dans le sens inverse : du pôle négatif au pôle positif.
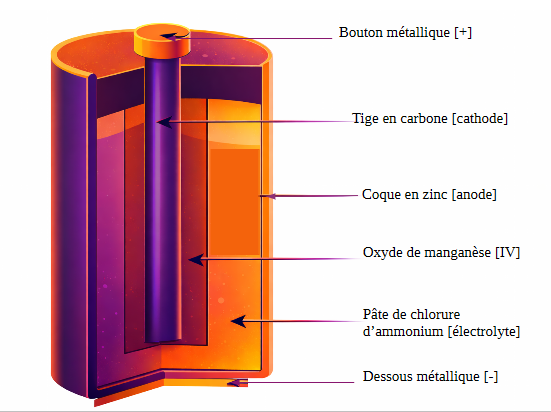
3. Les piles usuelles
On peut évoquer par exemple :
La pile saline ;
La pile alcaline ;
La pile à combustible ;
Etc.
II. Différence entre les piles et les accumulateurs
Pour rappel, une pile est un dispositif électrochimique qui convertit l'énergie chimique en énergie électrique. Elle fonctionne grâce à une réaction d'oxydoréduction spontanée et ne peut pas être rechargée.
Un accumulateur est un système électrochimique qui peut être rechargé en lui fournissant de l'énergie électrique, permettant de stocker de l'énergie chimique pour une utilisation ultérieure.
Différences fondamentales entre une pile et un accumulateur :
Une pile est à usage unique (non rechargeable) ;
Un accumulateur est rechargeable et peut subir plusieurs cycles de charge et décharge.
Exemples :
Une pile AA alcaline est jetable après utilisation ;
Une batterie de smartphone (accumulateur lithium-ion) peut être rechargée des centaines de fois.
III. Quantité d'électricité débitée par une pile et quantités de matière mises en jeu
1. Quantité d'électricité débitée par une pile
La quantité d'électricité mise en jeu au cours du fonctionnement d'une pile est égale à la charge totale des électrons échangés :
avec
quantité d'électrons échangés au cours du fonctionnement d'une pile ;
la constante d'Avogadro ;
la charge élémentaire.
Le faraday est la valeur absolue de la charge d'une mole d'électrons ou quantité d'électricité transportée par une mole d'électrons :
Ainsi, .
La quantité d'électricité que fait circuler une pile qui débite un courant d'intensité pendant une durée est :
La capacité d'une pile est la quantité d'électricité maximale que cette pile peut fournir.
2. Quantités de matière mises en jeu : application
Enoncé :
Au cours du fonctionnement d'une pile Daniell, la masse de l'électrode du zinc diminue de en .
Quelle est l'intensité du courant constant débitée ?
Solution :
Le symbole conventionnel de la pile Daniell est ;
La masse de zinc consommée est ;
La durée de fonctionnement de la pile est ;
L'équation de la réaction qui se produit à l'électrode de zinc est ;
La quantité de matière de zinc qui a été consommée est :
La quantité de matière d'électrons qui a circulé est ;
La quantité d'électricité qui a circulé est ;
La pile a fait circuler cette quantité d'électricité pendant la durée donc l'intensité du courant débitée par la pile est :
Application numérique :
;
;
;
.
donc
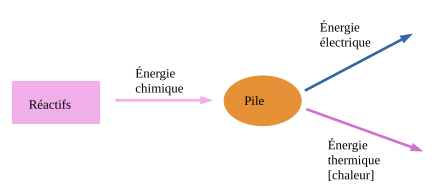
3. Conversion d'énergie chimique en énergie électrique
Dans une pile ou un accumulateur, la conversion d'énergie chimique en énergie électrique repose sur des réactions d'oxydoréduction qui se produisent aux électrodes.
Au niveau de l'anode, une oxydation se produit (perte d'électrons).
Au niveau de la cathode, une réduction se produit (gain d'électrons).
Les électrons circulent à travers un circuit externe, produisant un courant électrique.
La réaction globale peut s'écrire :
L'énergie chimique stockée est convertie en énergie électrique selon la relation :
où :
est l'énergie en joules (),
est la quantité d'électricité en coulombs (),
est la tension entre les bornes en volts ().
IV. Choix d'un système de stockage
1. Énergie totale stockée dans un accumulateur ou dans une pile
L'énergie totale stockée dans une batterie ou une pile peut être calculée à partir de ses caractéristiques techniques :
où :
est l'énergie stockée en wattheures (),
est la capacité de la batterie en ampères-heures (),
est la tension moyenne de fonctionnement en volts ().
Remarque : pour convertir cette énergie en joules :
Exemple d'application :
Une batterie de smartphone a une capacité de et une tension moyenne de .
Son énergie stockée est :
;
.
2. Caractéristiques principales des piles et accumulateurs
Tension à vide ou force électromotrice fém ( ou ) : tension aux bornes de la pile ou de l'accumulateur lorsqu'aucun courant ne circule.
Capacité () : quantité d'électricité que la pile ou l'accumulateur peut fournir avant d'être déchargé. Elle s'exprime en ampères-heures () ou en coulombs ().
Énergie massique : énergie stockée par unité de masse, exprimée en Wh/kg.
Énergie volumique : énergie stockée par unité de volume, exprimée en Wh/L.
Nombre de cycles de charge/décharge : Nombre de fois qu'un accumulateur peut être rechargé et déchargé avant que ses performances ne se dégradent significativement.
3. Choix d'un système de stockage
Le choix d'une pile ou d'un accumulateur dépend de plusieurs critères :
La tension requise par l'application ;
La capacité nécessaire pour une autonomie donnée ;
L'énergie massique ou volumique (poids et encombrement) ;
Le nombre de cycles de charge/décharge (pour les accumulateurs) ;
Le coût et la disponibilité ;
L'impact environnemental.
Exemples :
Pour un système embarqué nécessitant une tension de et une autonomie de avec un courant de :
La capacité requise est .
Le choix de la batterie dépendra des contraintes de poids, d'encombrement et de coût.
4. Applications concrètes
Il existe une multitude d'applications possibles pour le présent cours, y compris pour un sujet d'oral :
Choix des piles ou accumulateurs en fonction d'un cahier des charges donné : comparer les caractéristiques de différentes piles ou accumulateurs pour une application spécifique (exemple : télécommande, véhicule électrique).
Systèmes embarqués : analyser les contraintes énergétiques des systèmes embarqués (drones, capteurs, etc.) et choisir une solution de stockage adaptée.
Étude comparative de batteries de véhicules électriques ou hybrides : comparer les technologies de batteries (lithium-ion, nickel-métal hydrure) en termes de densité d'énergie, de durée de vie et de coût.
En effet, la miniaturisation des usages (smartphones, lunettes connectées, etc.) ou encore la quête d'une autonomie accrue conduisent à des contraintes plus importantes en termes de conception, et ce avec un coût raisonnable pour l'utilisateur, avec un impact le plus restreint possible pour l'environnement (extraction des matières premières, recyclage, etc.).
= Merci à gbm pour avoir contribué à l'élaboration de cette fiche =