I. Les changements d'état d'un corps pur
L'essentiel de ces notions ont déjà été introduites en classe de seconde dans la fiche de cours suivante :
1. Définition
Un changement d'état est une transformation physique au cours de laquelle une espèce passe d'un état physique (solide, liquide ou gazeux) à un autre.
Remarque : cette transformation est accompagnée d'un échange d'énergie thermique avec le milieu extérieur.
2. Rappels - Modélisation MACROSCOPIQUE d'un changement d'état
Remarque importante : les états physiques et les changements d'état ont été largement abordés en classe de 5e, il est donc fortement recommandé de relire attentivement cette fiche :
Définitions :
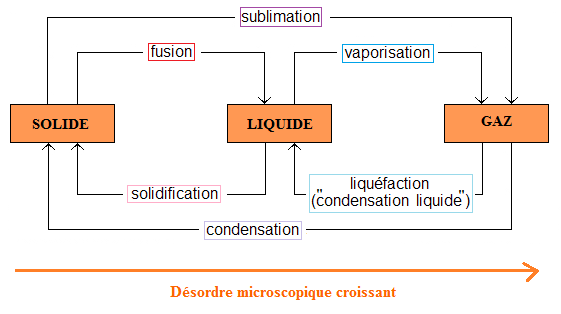
Chaque changement d'état porte un nom qui lui est propre :
Le passage de l'état solide à l'état liquide est appelé la FUSION ;
Le passage de l'état liquide à l'état solide est à contrario appelé la SOLIDIFICATION ;
Le passage de l'état liquide à l'état gazeux est appelé l’ÉVAPORATION ;
Le passage de l'état gazeux à l'état liquide est à contrario appelé la LIQUÉFACTION (souvent désignée abusivement par "condensation" dans le langage courant) ;
Le passage de l'état gazeux à l'état solide est appelé la CONDENSATION ;
Le passage de l'état solide à l'état gazeux est à contrario appelé la SUBLIMATION.
Quelques exemples (notamment issus de la fiche de 5e) :
Un glaçon qui fond dans un verre est une transformation physique : il passe de l'état solide à l'état liquide, c'est ce qu'on appelle une fusion ;
Un pot fermé, rempli de vapeur d'eau, plongé dans un bain de glace voit de l'eau liquide se former, qui se dépose au fond de ce pot : c'est une liquéfaction ;
Lorsque le volume d'eau de cuisson diminue dans une casserole : il s'agit d'une vaporisation ;
Le givre qui se forme sur une voiture l'hiver correspond à une solidification ;
Etc.
ATTENTION :
Il ne faut pas confondre la fusion (= passage de l'état solide à l'état liquide) et la dissolution (= action de dissoudre un soluté) !
Par exemple, il ne faut pas dire ou écrire que "le sucre fond dans le café/thé" mais bien que "le sucre se dissout dans le café". En effet, ce dernier ne subit pas de changement d'état, il ne fait que se disperser dans la boisson.
Propriétés :
Le nombre et la nature des espèces chimiques intervenant dans un changement d'état ne varient pas : la masse reste en effet constante.
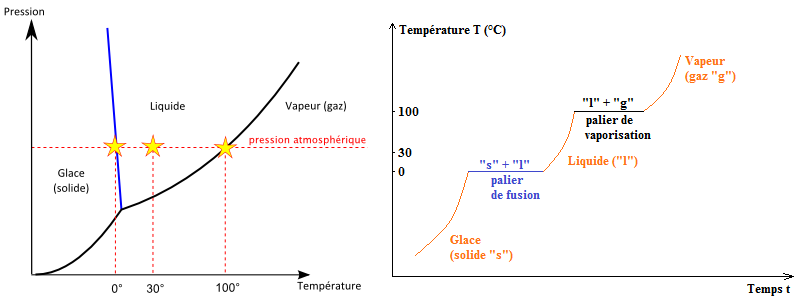
Lors d'un changement d'état d'un corps pur, la température reste constante : il y a des paliers de température qui sont caractéristiques de la substance.
À ces températures particulières, les deux états coexistent simultanément
Définition :
Un diagramme d'état représente les conditions de pression et de température pour lesquelles un corps pur existe sous un état physique donné (solide, liquide, gazeux).
Ce diagramme permet de déterminer l'état final d'un fluide lors d'une transformation physique, en fonction de sa pression et de sa température initiale et finale.
Points clés d'un diagramme d'état :
Point triple : point où les trois états coexistent ;
Point critique : au-delà de ce point, le liquide et le gaz ne peuvent plus être distingués (fluide supercritique) ;
Courbes de coexistence : courbes où deux états coexistent (fusion, vaporisation, sublimation).
Exemple : on considère un glaçon d'eau pure et qu'on augmente progressivement sa température au cours du temps, à pression constante, on obtiendra le graphique suivant :
3. Modélisation MICROSCOPIQUE d'un changement d'état
Un solide pur n'est constitué que d'un seul type d'atomes (ou molécules) ; il est modélisé par un ensemble d'atomes (ou molécules) qui sont "serrés" les uns contre les autres et soudés ensemble. On dit que l'état solide est compact et ordonné.
Un liquide pur n'est constitué que d'un seul type d'atomes (ou molécules) ; il est modélisé par un ensemble d'atomes qui sont "tassés" mais ils peuvent "glisser" les uns sur les autres. On dit que l'état liquide est compact et désordonné.
Un gaz pur n'est constitué que d'un seul type d'atomes (ou molécules) ; il est modélisé par un ensemble d'atomes peu nombreux, libres, en mouvement rapide et désordonné. On dit que l'état gazeux est dispersé et très désordonné.
Propriété :
Dans un changement d'état :
Une augmentation de la température entraîne un accroissement de l'agitation des atomes (ou des molécules) de l'espèce chimique considérée ;
Réciproquement, une diminution de la température entraîne une décroissance de l'agitation des atomes (ou molécules) de l'espèce chimique considérée.
4. Synthèse - Modélisation MACROSCOPIQUE d'un changement d'état
Remarque : dans le cas de l'eau, les liaisons hydrogène entre les molécules jouent un rôle clé dans les changements d'état. Par exemple, lors de la fusion de la glace, les liaisons hydrogène se rompent partiellement, ce qui nécessite un apport d'énergie thermique.
5. Écriture symbolique d'un changement d'état
À retenir :
L'écriture d'un changement d'état d'une espèce chimique se note avec la formule chimique de cette espèce, accompagnée de l'état physique en indice et entre parenthèses.
Notation : on utilisera un "" pour désigner l'état solide, un "" pour désigner l'état liquide et un "" pour désigner l'état gazeux.
Exemple : l'eau passant de l'état solide, à l'état liquide puis enfin à l'état gazeux, aura pour équation de changement d'état :
II. Aspects énergétiques d'une transformation physique
1. Notion de transfert thermique
Définition :
Le transfert thermique () est une énergie échangée sous forme de chaleur par l'espèce chimique qui subit le changement d'état avec le système considéré ;
Son unité est le joule ().
Le système est l'ensemble d'espèces chimiques étudié lors de la transformation physique.
Tout ce qui n'appartient pas au système est le milieu extérieur.
L'ensemble du système et du milieu extérieur constitue ce qu'on appelle "l'Univers".
Par convention :
Si l'espèce reçoit de la chaleur alors le transfert thermique sera positif :
A l'inverse, si l'espèce cède de la chaleur alors le transfert thermique sera négatif :
2. Transformations endothermiques et exothermiques
Définitions :
Un changement d'état endothermique est une transformation au cours de laquelle le système absorbe de l'énergie (). Généralement, cela se traduit par une diminution de sa température.
Un changement d'état exothermique est une transformation au cours de laquelle le système libère de l'énergie (). Généralement, cela se traduit par une augmentation de sa température.
Ainsi, expérimentalement, on peut observer que :
Lors d'une fusion, d'une vaporisation ou d'une sublimation, la transformation du système est endothermique ;
Lors d'une solidification, d'une liquéfaction ou d'une condensation, la transformation du système est exothermique.
3. Énergie de changement d'état
Définition :
Lors d'un changement d'état, l'énergie liée à cette transformation est appelée énergie massique de changement d'état ou chaleur latente, notée .
Elle est caractéristique de l'espèce considérée.
Elle correspond à la quantité d'énergie que le système doit absorber ou céder pour qu'une masse de l'espèce chimique considérée change d'état :
où :
est l'énergie thermique échangée en kilojoules () ;
est la masse du corps pur en kilogrammes () ;
est l'énergie massique de changement d'état (ou chaleur latente) en kilojoules par kilogramme ().
Expérimentalement, on peut observer que :
Les chaleurs latentes de fusion, de vaporisation et de sublimation sont positives ;
Les chaleurs latentes de solidification, de liquéfaction et de condensation sont négatives ;
Ainsi, pour une même espèce, les chaleurs latentes de changements d'état opposés (par exemple vaporisation vs liquéfaction) sont égales en valeur absolue, mais de signes contraires.
4. Application : la calorimétrie
En pratique, la détermination de l'énergie latente peut s'effectuer dans un calorimètre.
En effet, ce dernier a la propriété de n'échanger presque aucune énergie avec l'extérieur.
Ainsi, idéalement, on peut considérer que la somme de tous les échanges de chaleur à l'intérieur d'un calorimètre est nulle.
III. Bilan énergétique d'une transformation physique
1. Inventaire d'une énergie de changement d'état
Comme cela a été vu précédemment, lorsqu'un corps pur subit un changement d'état, il échange une quantité d'énergie thermique appelée énergie massique de changement d'état (ou chaleur latente). Cette énergie est nécessaire pour rompre ou établir les liaisons entre les molécules.
L'énergie de changement d'état (en ) s'exprime donc de la façon suivante :
Valeurs typiques pour l'eau :
Chaleur latente de fusion () : ;
Chaleur latente de vaporisation () : .
Exemple :
Pour faire fondre de glace à sous pression atmosphérique, l'énergie nécessaire est :
2. Capacité thermique massique
Cette notion a été introduite en classe de première dans la fiche de cours suivante :
Pour rappel, la capacité thermique massique représente la quantité d'énergie nécessaire pour élever la température d'une masse de d'un corps pur de .
L'énergie thermique nécessaire pour chauffer ou refroidir un corps pur sans changement d'état s'exprime de la façon suivante :
où :
est l'énergie thermique en joules () ;
est la masse du corps pur en kilogrammes () ;
est la capacité thermique massique en joules par kilogramme-kelvin () ;
est la variation de température en kelvins () ou en degrés Celsius ().
Valeur typique pour l'eau : .
Exemple :
Pour chauffer d'eau de à , l'énergie nécessaire est :
3. Bilan énergétique complet d'une transformation physique
Méthode :
Pour établir un bilan énergétique complet d'un système subissant plusieurs transformations physiques (un chauffage, un refroidissement ou encore un changement d'état), il suffit de faire l'inventaire des énergies mises en jeu pour chaque étape, puis de les additionner.
Hypothèse fondamentale :
A l'image d'un calorimètre, le système est supposé n'échanger presque aucune énergie avec l'extérieur. Ainsi, idéalement, on peut considérer que la somme de tous les échanges de chaleur à l'intérieur d'un calorimètre est nulle.
Remarque :
Généralement ces systèmes sont calorifugés, de manière à limiter - autant que faire se peut - les échanges thermiques avec le milieu extérieur.
Exemple :
Pour transformer de glace à en vapeur à à pression atmosphérique, les étapes sont :
1. Réchauffer la glace de à ;
2. Faire fondre la glace à ;
3. Réchauffer l'eau liquide de à ;
4. Vaporiser l'eau à ;
5. Réchauffer la vapeur d'eau de à .
Le bilan énergétique total est la somme des énergies pour chaque étape.
IV. Applications concrètes
Il existe une multitude d'applications possibles pour le présent cours, y compris pour un sujet d'oral :
Étude des systèmes de chauffage et de climatisation :
Analyser le fonctionnement d'une pompe à chaleur ou d'un climatiseur, en termes de transferts thermiques et de changements d'état du fluide frigorigène ;
Calculer les énergies mises en jeu et l'efficacité énergétique de ces systèmes.
Étude des procédés industriels :
Analyser les changements d'état dans les procédés de distillation, de lyophilisation, ou de cryogénie ;
Calculer les bilans énergétiques pour optimiser ces procédés.
En effet, l'établissement de ces bilans énergétiques permet d'étudier les possibilités d'optimisation des systèmes pour atteindre les objectifs de sobriété énergétique de la France d'ici 2050.
= Merci à gbm pour avoir contribué à l'élaboration de cette fiche =