Introduction
Lors d’un accident de voiture, chaque seconde compte. L’activation rapide d’un airbag ou la détection de substances comme l’alcool dans le sang peuvent faire la différence entre la vie et la mort. La chimie joue un rôle central dans ces dispositifs de sécurité. Comprendre comment une réaction chimique permet de gonfler un airbag en quelques millisecondes ou comment un alcootest identifie la présence d’alcool repose sur des notions simples mais essentielles comme les transformations chimiques, le bilan de matière ou encore le volume molaire. Ces concepts permettent également d’expliquer les méthodes utilisées pour détecter la présence de substances illicites dans l’organisme.
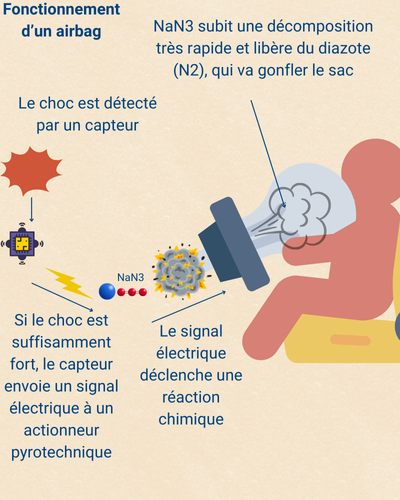
Fonctionnement chimique d’un airbag
Lors d’un choc violent, un signal électrique déclenche une réaction chimique à l’intérieur de l’airbag. Cette réaction produit un gaz qui gonfle le coussin en un temps très court, protégeant ainsi le conducteur et les passagers.
L’airbag contient un composé solide comme l’azoture de sodium (). Lorsqu’il est chauffé, il subit une décomposition très rapide selon la réaction :
Le diazote () formé est un gaz qui se répand instantanément dans le sac, le gonflant.
Pour comprendre quantitativement ce processus, on utilise la notion de volume molaire. Dans les conditions normales de température et de pression (CNTP), le volume molaire est d’environ . Le volume de gaz produit est donc donné par la relation :
où est la quantité de matière en moles. Un calcul rapide permet d’ajuster la masse de NaN₃ nécessaire pour obtenir un volume de diazote suffisant afin de gonfler l’airbag à la bonne taille.
À retenir
Un airbag se gonfle grâce à une décomposition chimique rapide produisant du diazote. Le volume de gaz obtenu dépend de la quantité de matière et du volume molaire selon la relation .
Principe chimique de l’alcootest
L’alcootest repose sur une réaction d’oxydoréduction. Dans un appareil classique, l’éthanol () contenu dans l’air expiré est oxydé en acide acétique () par un oxydant puissant, le dichromate de potassium (), en milieu acide.
Le dichromate est un ion polyatomique () de couleur orange qui contient du chrome à l’état d’oxydation . Au cours de la réaction, il est réduit en ion chrome(III) (), de couleur vert. Cette transformation est à l’origine du changement de couleur observé.
La réaction globale simplifiée peut s’écrire :
Ce changement de couleur (orange → vert) est exploité dans les alcootests chimiques. Dans les modèles électroniques, un capteur mesure un courant électrique proportionnel à la concentration d’éthanol.
À retenir
L’alcootest utilise une réaction d’oxydoréduction : l’éthanol est oxydé et le dichromate est réduit. Le changement de couleur ou la mesure d’un courant permet d’évaluer la concentration d’alcool.
Détection de substances illicites dans l’organisme
La détection de drogues ou de médicaments non autorisés peut se faire à partir d’échantillons biologiques comme l’urine, le sang ou la salive. Ces analyses reposent sur des principes chimiques variés :
Chromatographie : séparation des composants d’un mélange selon leurs interactions avec un support et un solvant. Chaque substance possède un temps de rétention caractéristique.
Spectrométrie de masse : identification des molécules par mesure de leur masse et de leur structure.
Réactions colorimétriques : certaines drogues réagissent avec des réactifs spécifiques produisant un changement de couleur détectable.
Ces méthodes permettent d’identifier des traces infimes de substances et d’établir un profil toxicologique fiable.
À retenir
Les substances illicites sont détectées grâce à des méthodes analytiques (chromatographie, spectrométrie de masse, tests colorimétriques) capables d’identifier des molécules spécifiques même à très faible concentration.
Conclusion
La chimie est au cœur de nombreux dispositifs qui garantissent la sécurité routière. De l’airbag qui se gonfle en un instant grâce à une réaction chimique au contrôle de l’alcoolémie par oxydoréduction, en passant par la détection des drogues, chaque technologie repose sur des principes chimiques précis. Ces avancées permettent de mieux prévenir les accidents et de renforcer la sécurité de tous les usagers de la route.