I. Les ondes électromagnétiques (modèle ondulatoire)
Les ondes électromagnétiques ont été abordées en détail dans la fiche de cours suivante :
II. La mécanique newtonienne et ses limites
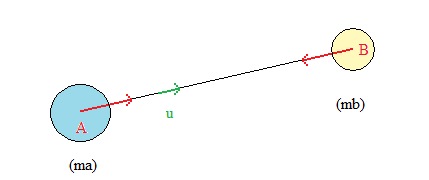
1. La force gravitationnelle : loi de gravitation universelle
Loi de Newton (rappel) :
"Deux corps et B répartition sphérique de masse, de masses et , dont les centres sont séparés par la distance , exercent l'un sur l'autre des forces attractives de même valeur, proportionnelles aux masses et inversement proportionnelles au carré de la distance qui les séparent" :
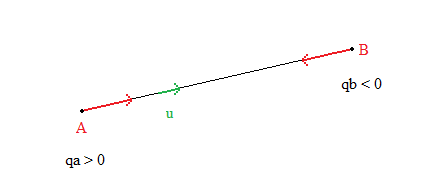
2. La force électrostatique : la loi de Coulomb
Loi de Coulomb (hors programme) :
"Deux charges ponctuelles et , placées aux points et distants de , exercent l'une sur l'autre des forces répulsives pour des charges de même signe, attractives pour des charges de signes contraires, de même valeur" :
3. Remarque
Dans un atome, par exemple dans l'atome d'hydrogène, la force gravitationnelle est négligeable par rapport à la force électrostatique qui agit sur l'électron.
4. Comparaison des systèmes planétaires et des cortèges électroniques des atomes
Les systèmes planétaires et les atomes présentent une grande similitude : un objet central autour duquel se déplacent d'autres objets soumis à une force centripète.
Pourtant, il existe des différences fondamentales entre ces deux systèmes :
Les systèmes planétaires présentent une grande diversité : tous les rayons orbitaux sont possibles pour les planètes et les satellites.
Tous les atomes d'un même élément chimique sont identiques, ils ont tous le même rayon. Par conséquent, les électrons occupent un espace identique pour tous les atomes d'une même espèce chimique.
La mécanique newtonienne ne permet donc pas de justifier l'identité des atomes.
III. Quantification des niveaux d'énergie électroniques d'un atome (modèle corpusculaire)
1. Spectres atomiques
Définitions :
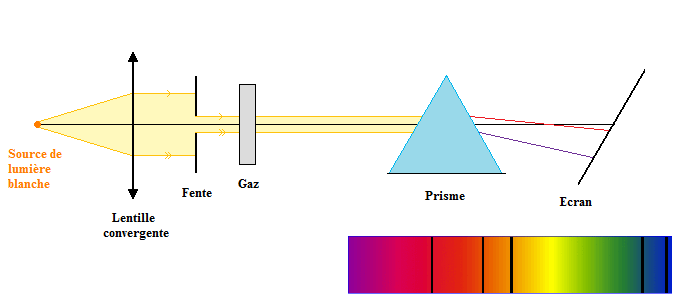
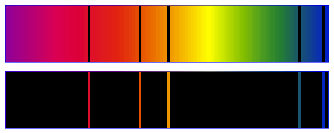
Le spectre d'une lumière est la séparation des radiations monochromatiques qui constituent cette lumière à l'aide d'un prisme.
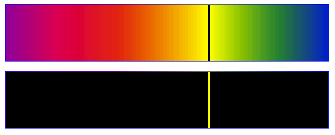
On a un spectre de raies si la plage colorée sur l'écran est discontinue ; on dit qu'elle présente des raies.
Un spectre d'émission est le spectre de la lumière émise par de la matière excitée. En effet, la matière qui a reçu de l'énergie sous forme calorifique, électrique, mécanique, lumineuse, etc. émet de la lumière.
Un spectre d'absorption est le spectre de la lumière blanche dont certaines radiations ont été absorbées lors de la traversée d'une matière.
Exemples : spectre d'émission avec une lampe à vapeur de sodium ou de mercure :
On observe des raies colorées brillantes sur fond noir.
Ces raies colorées sont caractéristiques de l'atome excité.
Le spectre de la lumière émise par un gaz sous faible pression et à haute température (donc constitué d'atomes) est un spectre de raies.
Propriété :
Les atomes excités émettent un rayonnement pour certaines fréquences seulement (ces atomes se désexcitent en émettant de l'énergie lumineuse).
Remarque : le spectre de la lumière blanche émise par le filament incandescent d'une lampe est un spectre continu.
Spectre d'absorption :
On observe des raies noires dans le spectre de la lumière blanche (arc-en-ciel).
Ces raies noires sont celles des radiations monochromatiques qui ont été absorbées par le gaz.
Remarques :
Les fréquences des couleurs absorbées par un atome sont les mêmes que celles qui sont émises par un atome quand il est excité.
Pour le sodium (spectres d'absorption et d'émission) :
Pour le mercure (spectres d'absorption et d'émission) :
Le spectre devient de plus en plus compliqué quand le numéro atomique de l'atome augmente.
2. Niveaux d'énergie des atomes
Pour expliquer le "caractère discret" des fréquences émises ou absorbées par un atome (c'est-à-dire quand l'atome ne peut émettre ou absorber que certaines couleurs), des postulats ont été émis concernant l'échange d'énergie entre l'atome et la lumière.
En 1900, Max Planck a postulé : "l'énergie transportée par les ondes électromagnétiques émises ou absorbées par un atome est quantifiée, c'est-à-dire qu'elle ne peut s'échanger que par paquets ou quanta d'énergie".
En 1905, Albert Einstein a postulé : "ces quanta d'énergie sont portés par des particules appelées photons".
Pour une onde électromagnétique de fréquence , de longueur d'onde et de célérité dans le vide, l'énergie d'un photon est :
où est la constante de Planck et la célérité de la lumière dans le vide .
Le photon est un corpuscule de masse nulle, de charge nulle, qui se propage à la célérité de la lumière dans le vide ou l'air.
Unités S.I : est en ; est en ; est en ; est en ; est en .
En 1913, Niels Bohr énonce deux postulats :
1er postulat :
L'énergie d'un atome est quantifiée.
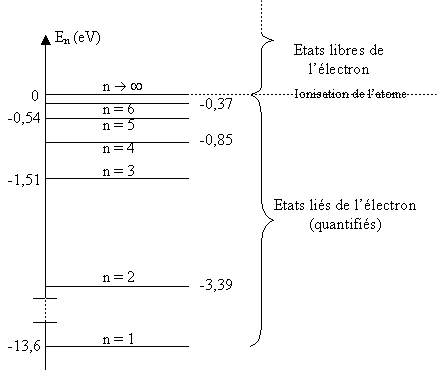
L'énergie d'un atome ne peut prendre que certaines valeurs bien déterminées. On dit que l'atome ne peut exister que dans un nombre discret de niveaux d'énergie.
Chaque niveau d'énergie de l'atome correspond à un état de l'atome, c'est-à-dire à une répartition des électrons autour du noyau :
L'état fondamental de l'atome est l'état de plus basse énergie pour lequel les électrons sont le plus liés au noyau.
Un état excité de l'atome est un état de l'atome qui a absorbé de l'énergie, donc pour lequel les électrons sont moins liés au noyau que dans l'état fondamental.
L'état ionisé de l'atome est l'état pour lequel l'atome a perdu un électron.
Diagramme des niveaux d'énergie d'un atome (par exemple pour l'hydrogène)
2e postulat :
Les variations d'énergie d'un atome sont quantifiées.
Le passage d'un niveau d'énergie à un autre, appelé transition, s'accompagne de l'émission ou de l'absorption d'un photon.
L'énergie du photon émis ou absorbé (constante de Planck x fréquence) est égale à la variation de l'énergie de l'atome :
Représentation avec un diagramme d'énergie
Remarque :
L'électronvolt est défini comme l'énergie cinétique acquise par un électron accéléré sous une différence de potentiel électrique (= tension) de :
L'électronvolt permet d'exprimer simplement les énergies des photons, des électrons dans un atome, ou encore les énergies de liaison entre particules. Il est donc primordial de savoir faire cette conversion d'unité !
IV. Effet photoélectrique et conversion photovoltaïque
1. Définition
Dans le § précédent, il a été rappelé que l'atome ne peut exister que dans dans un nombre discret de niveaux d'énergie, chaque niveau d'énergie de l'atome correspond à un état de l'atome, c'est-à-dire à une répartition des électrons autour du noyau : l'état fondamental, l'état excité et l'état ionisé.
L'effet photoélectrique est un phénomène physique dans lequel des électrons sont émis par un matériau, généralement un métal, lorsqu'il est exposé à la lumière ou à un autre rayonnement électromagnétique d'une certaine fréquence.
C'est en 1839 qu'est découvert l’effet photoélectrique par le physicien français Antoine Becquerel (le grand-père du découvreur de la radioactivité).
2. Analyse qualitative de l’effet photoélectrique
Lorsqu'un rayonnement électromagnétique (correspondant à un flux de photons) frappe la surface d'un matériau, elle peut transférer son énergie aux électrons de ce dernier. Si l'énergie de la lumière est suffisante, elle peut arracher des électrons de sa surface.
Propriété :
Il existe une fréquence minimale du rayonnement, appelée fréquence de seuil, en dessous de laquelle aucun électron n'est émis, peu importe l'intensité de ce rayonnement. Cela montre que l'effet photoélectrique dépend de la fréquence de la lumière et non de son intensité.
Ainsi, l'énergie cinétique des électrons émis dépend de la fréquence du rayonnement incident et non de son intensité. Un rayonnement de fréquence plus élevée libère des électrons avec une énergie cinétique plus élevée.
3. Applications industrielles de l'effet photoélectrique
Les applications industrielles ont été abordées en détail dans la fiche de cours suivante :
L'énergie transportée par la lumière
4. La cellule photovoltaïque : fonctionnement et principe
Le fonctionnement et le principe d'une cellule photovoltaïque ont été abordés en détail dans la fiche de cours suivante :
L'énergie transportée par la lumière
La puissance par du rayonnement solaire reçu à la surface de la Terre est de l’ordre de , valeur dépendant de la latitude, de la saison et des conditions météorologiques.
La puissance des installations est exprimée en watt-crête (). Le watt-crête est la puissance fournie par un module photovoltaïque pour un ensoleillement normalisé de à une température de .
Les puissances mises en jeu dans une conversion photovoltaïque sont :
Puissance lumineuse (celle des photons incidents) ;
Puissance électrique produite (courant et tension générés) ;
Puissance thermique dissipée (pertes par échauffement de la cellule).
Le rendement d’une cellule photovoltaïque est le rapport entre la puissance électrique produite par cette cellule et la puissance lumineuse reçue sur sa surface :
la tension délivrée par la cellule (en ) ;
l’intensité du courant délivrée par la cellule (en ) ;
l'énergie lumineuse reçue sur la surface de la cellule (en ) ;
la surface de cette cellule (en ).
Courbe caractéristique d'une cellule photovoltaïque :

Matériau de la cellule : différents matériaux semi-conducteurs ont des rendements différents. Par exemple, les cellules en silicium monocristallin ont généralement un rendement plus élevé que celles en silicium polycristallin.
Les cellules photovoltaïques commerciales ont généralement un rendement compris entre et ;
Les cellules à haut rendement, comme celles utilisées dans les applications spatiales, peuvent atteindre des rendements de plus de ;
Ces faibles rendements sont dus aux pertes (réflexion des rayons incidents, pertes par effet Joule, etc.) et au fait que la sensibilité de la cellule ne couvre pas la totalité du spectre du rayonnement solaire (le seuil de conduction déterminé par une énergie de pour le silicium cristallin, correspondant à une fréquence de , soit un rayonnement infrarouge).
Conditions d'ensoleillement : l'intensité et le spectre de la lumière solaire peuvent affecter le rendement.
Température : les cellules photovoltaïques peuvent voir leur rendement diminuer à des températures élevées.
V. La conversion photothermique
La conversion photothermique est le processus par lequel l'énergie lumineuse est convertie en énergie thermique, généralement par absorption de la lumière dans un matériau.
Dans un capteur solaire thermique, la lumière est absorbée par une surface noire, augmentant sa température. Cette chaleur est ensuite transférée à un fluide caloporteur (eau voire huile) qui circule dans le capteur.
Les puissances mises en jeu dans une conversion photothermique sont :
Puissance lumineuse (celle des photons incidents) ;
Puissance thermique (chaleur générée dans le capteur),
Puissance mécanique (si le fluide caloporteur entraîne une turbine).
Le rendement d’une cellule photothermique est le rapport entre la puissance thermique générée par cette cellule et la puissance lumineuse reçue sur sa surface :
puissance thermique générée par la cellule (en ) ;
l'énergie lumineuse reçue sur la surface de la cellule (en ) ;
la surface de cette cellule (en ).
VI. Applications concrètes
Il existe une multitude d'applications possibles pour le présent cours, y compris pour un sujet d'oral :
Comparaison du rendement de conversion de divers panneaux solaires photovoltaïques : analyser les caractéristiques et les performances des panneaux monocristallins, polycristallins et amorphes en termes de rendement, de coût et d'adaptation aux conditions climatiques.
Étude de l'autonomie énergétique d'une habitation équipée de panneaux solaires thermiques et photovoltaïques : dimensionner une installation solaire pour couvrir les besoins énergétiques d'une habitation, en tenant compte des variations saisonnières et des conditions d'ensoleillement.
La voile solaire : étudier le principe de propulsion d'une voile solaire, où la pression de radiation de la lumière solaire est exploitée pour propulser un vaisseau spatial sans carburant.
En effet, les enjeux énergétiques ont été revus dans la fiche de cours suivante :
= Merci à gbm pour avoir contribué à l'élaboration de cette fiche =