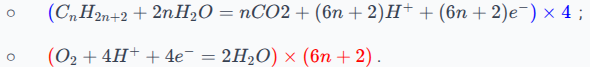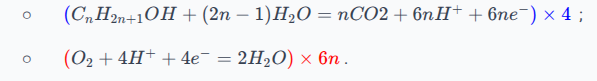I. Étude qualitative des transformations chimiques : rappels
1. Prérequis
Les notions liées à l'étude qualitative des transformations (ou réactions) chimiques ont été abordées en classe de seconde.
Aussi est-il recommandé de réviser la fiche suivante :
Cette première partie ne propose qu'une synthèse des principales notions à retenir.
2. Notion d'évolution d'un système chimique
Un système chimique (ou milieu réactionnel) est un mélange d'espèces chimiques qui sont susceptibles de réagir entre elles.
Pour caractériser un système chimique, il est nécessaire de définir l'ensemble des paramètres le constituant, c'est-à-dire :
Les conditions de réalisation de la transformation : la température et la pression ;
Toutes les espèces chimiques mises en jeu avec, pour chacune d'elles, leurs formules brutes et leur(s) état(s) physique(s) ;
Les quantités de matière de chacune des espèces chimiques mises en jeu (= bilan de matière).
Tous ces paramètres définissent ce qu'on appelle l'état d'un système chimique.
Remarque : les transformations chimiques usuelles se font généralement à l'air libre (sous la pression atmosphérique).
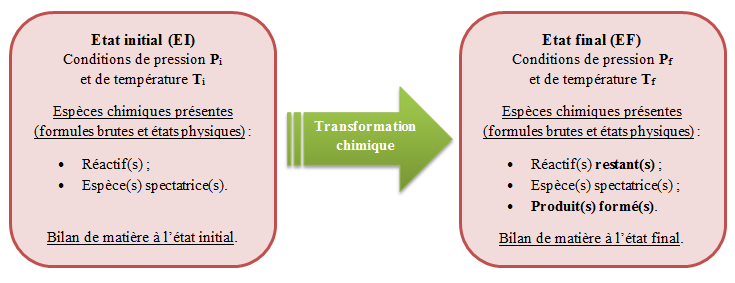
La transformation (ou réaction) chimique est une évolution d'un système chimique au cours de laquelle des espèces chimiques disparaissent (= réactifs), tout en laissant apparaître de nouvelles espèces chimiques (= produits) ;
Cette caractérisation de l'évolution est permise par la comparaison d'un état initial avec un état final, lorsqu'il n'y a plus de réaction ;
Les espèces chimiques présentes dans le système mais n'étant pas affectées par la transformation sont dites spectatrices.
3. Caractérisation d'une transformation chimique
"Rien ne se perd, rien ne se créé, tout se transforme" une transformation chimique est caractérisée par une conservation de la matière. Elle se traduit de deux manières :
Conservation de la masse totale du système (autrement dit, conservation du nombre d'atomes des éléments chimiques constituant le système) ;
Conservation de la charge globale du système.
Aspects énergétiques :
Une réaction endothermique est une transformation au cours de laquelle le système chimique (ou milieu réactionnel) absorbe de l'énergie. Généralement, cela se traduit par une diminution de sa température ;
Une réaction exothermique est une transformation au cours de laquelle le système chimique (ou milieu réactionnel) libère de l'énergie. Généralement, cela se traduit par une augmentation de sa température.
L'équation d'une réaction chimique permet d'établir le bilan des réactifs intervenant dans cette transformation et les produits formés par cette réaction :
Par le biais de leur formules chimiques ;
En précisant l'état physique de chaque espèce intervenant dans la réaction : solide , liquide , gazeux ou aqueux ;
En indiquant également les proportions des quantités qui interviennent (mais pas les conditions de pression et de température dans lesquelles se déroule la réaction).
Exemple : soit l'équation générale d'une réaction chimique .
A l'échelle microscopique : espèce(s) chimique(s) (atome(s), molécule(s) ou ion(s)) réagissent avec espèce(s) chimique(s) pour former espèce(s) chimique(s) et espèce(s) chimique(s) ;
A l'échelle macroscopique : mole(s) de l'espèce chimique réagissent avec mole(s) de l'espèce chimique . Il se forme mole(s) de l'espèce chimique et mole(s) de l'espèce chimique .
Remarque importante : les espèces spectatrices, qui n'interviennent pas dans la réaction (c'est-à-dire ne réagissent pas) ne doivent pas apparaître dans l'équation-bilan.
L'équation-bilan étant représentative de la transformation étudiée, la propriété de conservation de la matière (en masse et en charge) doit donc être respectée la méthode d'équilibrage d'une équation-bilan doit donc être parfaitement maîtrisée !
En conséquence, il est nécessaire d'introduire devant chaque espèce chimique intervenante un nombre qu'on peut ajuster pour traduire cette conservation : on l'appelle le coefficient stœchiométrique.
L'analyse des proportions entre les espèces engagées (= réactifs) et les espèces formées (= produits) est la stœchiométrie.
II. Combustion des matières organiques
1. Notion de combustion
Définition :
Une combustion est une transformation chimique d'oxydoréduction au cours de laquelle le système libère de l'énergie : c'est une réaction exothermique. Elle s'accompagne donc d'une hausse systématique de température du milieu extérieur.
2. Réactifs et produits d'une combustion
Une combustion se caractérise par le contact de deux réactifs :
Le combustible, qui est l'espèce chimique qui brûle ; c'est celui des réactifs qui a subi une oxydation.
Le comburant, qui est l'espèce chimique qui aide le combustible à brûler (généralement il s'agira du dioxygène ). C'est celui des réactifs qui a subi une réduction.
Propriété :
Lors d'une combustion complète, tout le combustible a réagi (= réaction totale, le dioxygène étant généralement en excès) et les produits formés sont le dioxyde de carbone () et l'eau ().
Remarque : en présence d'un comburant, il faut apporter une quantité d'énergie pour initier une réaction de combustion, et donc l'inflammation d'un combustible : il s'agit de l'énergie d'activation.
Le combustible, le comburant et l'énergie d'activation sont souvent représentés de manière symbolique par le triangle du feu. En effet, la combustion cesse dès qu’un élément du triangle est enlevé.
3. Combustibles organiques usuels
Les combustibles utilisés dans la vie quotidienne sont essentiellement d'origine fossile. Ils résultent de la décomposition d'organismes vivants effectuée pendant plusieurs millions d'années.
Les alcanes et les alcools sont privilégiés comme combustibles car ils ont une forte énergie massique ou volumique :
Le gaz naturel est composé d'hydrocarbures gazeux constitués de méthane (en grande majorité), d'éthane , de propane et de butane . Il est rendu odorant par l'ajout de (tétrahydrothiophène) ;
Certaines cheminées ou poêles fonctionnent à l'éthanol .
II. Réaction de combustion des alcanes et des alcools
1. Réaction de combustion d'un alcane ou d'un alcool
Comme nous l'avons vu précédemment, la réaction de combustion d'un alcane ou d'un alcool est une réaction d'oxydoréduction entre l'une des deux espèces organiques et le dioxygène, les produits formés étant le dioxyde de carbone et l'eau.
Remarque : pour plus d'information sur une réaction d'oxydoréduction, se référer à la fiche suivante :
Ces réactions exothermiques s'effectuant à des températures élevées, on suppose que cette transformation entre ses réactifs et ses produits se fait à l'état gazeux.
3. Équation-bilan d'une réaction de combustion
Les couples en jeu sont :
;
.
Les demi-équations électroniques, dans le sens de la réaction effective, sont les suivantes :
;
.
On remarque que le nombre d'électrons n'est pas le même, on va donc multiplier la première demi-équation par et la deuxième demi-équation par , on aura donc électrons :
Finalement, l'équation de la réaction (une fois simplifiée) sera :
Les couples en jeu sont :
;
.
Les demi-équations électroniques, dans le sens de la réaction effective, sont les suivantes :
;
.
On remarque que le nombre d'électrons n'est pas le même, on va donc multiplier la première demi-équation par et la deuxième demi-équation par , on aura donc électrons :
Finalement, l'équation de la réaction (une fois simplifiée) sera :
Il ne sera pas nécessaire de refaire toutes les étapes d'écriture d'une équation-bilan d'oxydoréduction.
En effet, on peut équilibrer ces réactions directement en commençant par équilibrer le carbone et l'oxygène et en terminant par l'hydrogène, selon le principe de Lavoisier. Pour cela, il est conseillé de lire attentivement le §II. 4. de la fiche suivante :
Combustion du propane : (l'équilibrage de cette équation-bilan est détaillé dans la fiche ci-dessus) ;
Combustion de l'éthanol : .
III. Énergie libérée au cours d'une combustion
Définition :
Le pouvoir calorifique d'un alcane ou d'un alcool, noté correspond à l'énergie thermique libérée par une combustion complète de kg de combustible ;
C'est l'opposé de l'énergie libérée au cours d'une réaction de combustion par unité de masse.
C'est donc une grandeur positive, qui s'exprime généralement en ou .
Quelques valeurs usuelles :
;
;
;
;
Ces valeurs montrent que certains combustibles libèrent plus d'énergie que d'autres pour une même masse.
Expression :
Ainsi, pour une masse de combustible, l'énergie libérée par une combustion complète, notée vaut :
avec, généralement :
en ;
en ;
en ou .
Expérience pour déterminer le pouvoir calorifique :
Pour déterminer expérimentalement le pouvoir calorifique d’un combustible, on utilise par exemple un calorimètre ;
Le principe consiste à brûler une masse connue de combustible et à mesurer la quantité de chaleur dégagée, qui est absorbée par une quantité connue d’eau ;
La quantité de chaleur Q est calculée en utilisant la formule : , où est la masse d’eau, est la capacité thermique massique de l’eau et est la variation de température de l’eau.
Exemple d'application :
Si on brûle d'alcool et que cela provoque une augmentation de température de pour d’eau, on peut calculer la quantité de chaleur dégagée et en déduire le pouvoir calorifique de l'alcool.
IV. Combustions et enjeux de société
1. Dangers associés aux combustions
La dépendance de nos sociétés modernes aux énergies fossiles, ainsi que les dangers associés aux combustions ont été abordés dans la fiche de cours suivante (§VI. 2.) :
2. Moyens de prévention et de protection associés
Les combustions peuvent présenter plusieurs dangers :
Risque d'incendie : les combustibles peuvent s'enflammer et provoquer des incendies ;
Risque d'explosion : certains gaz combustibles peuvent exploser s'ils sont mélangés à l'air dans des proportions spécifiques ;
Intoxication par les fumées : la combustion peut produire des gaz toxiques comme le monoxyde de carbone () ;
Pollution de l'air : La combustion libère des polluants atmosphériques, comme le dioxyde de soufre (), les oxydes d'azote (), et le dioxyde de carbone ().
Voici quelques moyens de prévention et de protection contre les dangers des combustions :
Ventilation : assurer une bonne ventilation pour éviter l'accumulation de gaz combustibles ou toxiques.
Détecteurs de fumée et de gaz : installer des détecteurs de fumée et de monoxyde de carbone pour alerter en cas de danger.
Extincteurs : avoir des extincteurs adaptés aux types de feux potentiels (feux de solides, liquides, gaz).
Respect des consignes de sécurité : suivre les consignes de sécurité pour le stockage et l'utilisation des combustibles.
Équipements de protection individuelle (EPI) : utiliser des EPI, comme des gants et des lunettes de protection, lors de la manipulation de combustibles.
= Merci à gbm et à athrun pour avoir essentiellement contribué à l'élaboration de cette fiche =